Тезаморелин: GHRH аналог за висцерални мазнини и липодистрофия
Механизми, клинични доказателства и практически протоколи
Въведение
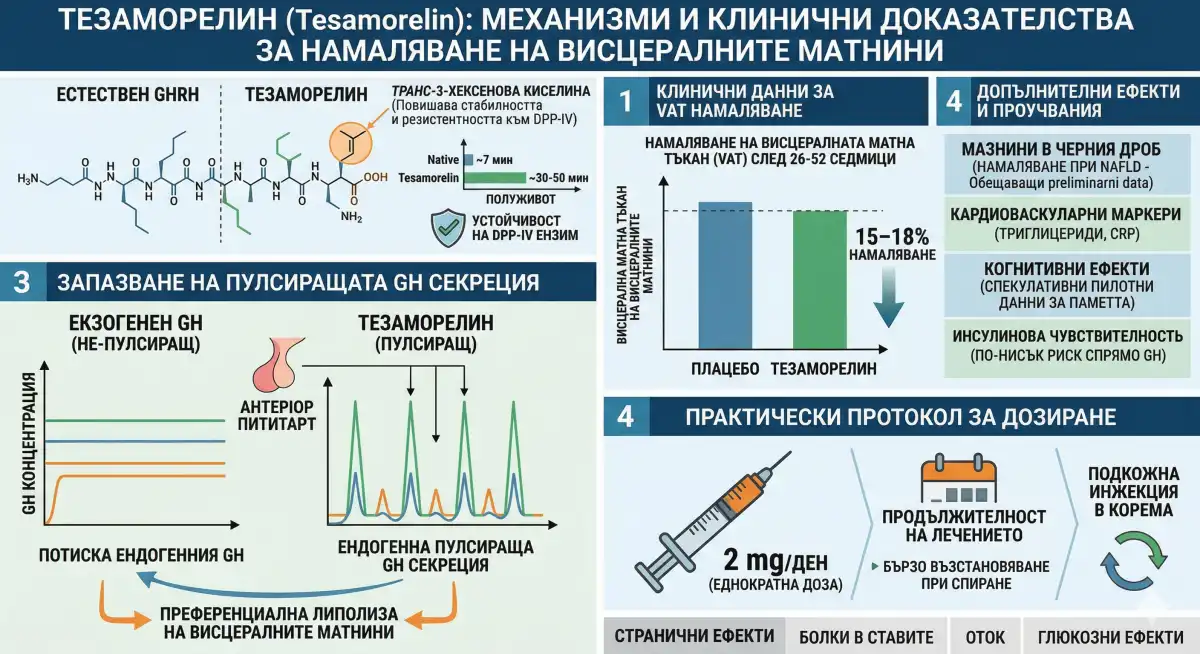
Тезаморелин е синтетичен аналог на хормона, освобождаващ растежен хормон (GHRH), отличаващ се с една структурна модификация — група на транс-3-хексенова киселина, прикрепена към тирозина на позиция 1. Тази модификация не е козметична. Тя придава устойчивост към дипептидил пептидаза-IV (DPP-IV), ензимът, който бързо разгражда естествения GHRH, като удължава полуживота от приблизително 7 минути до около 30–50 минути. Резултатът е съединение, достатъчно мощно и стабилно за еднократно дневно подкожно дозиране, което надеждно стимулира производството на ендогенен растежен хормон.
Предлаган на пазара като Egrifta, тезаморелин притежава одобрение от FDA за едно единствено показание: намаляване на излишните коремни мазнини при пациенти с ХИВ, страдащи от липодистрофия. Той е единственият GHRH аналог, подкрепен от клинични изпитвания Фаза 3 за намаляване на висцералните мазнини. Всичко отвъд това одобрено приложение — когнитивно подобряване, намаляване на чернодробните мазнини в общата популация, протоколи за дълголетие — варира от "обещаващи пилотни данни" до "спекулации в общността". Тази статия очертава доказателствата обективно.
Механизъм на действие: От рецептора до липолизата
Сигнализиране в хипофизата
Тезаморелин се свързва с GHRH рецептора (GHRHR), G-протеин свързан рецептор, експресиран върху соматотрофните клетки в предния дял на хипофизата. Активирането на рецептора задейства следната каскада:
- Активиране на Gαs протеин → стимулиране на аденилат циклазата
- Увеличаване на вътреклетъчния cAMP → активиране на протеин киназа А (PKA)
- Приток на калций през волтаж-зависими канали
- Екзоцитоза на секреторни гранули, съдържащи GH и повишаване на генната транскрипция на GH
Критично е, че този процес запазва пулсативния модел на секреция на GH. Хипоталамо-хипофизната верига за обратна връзка остава непокътната: соматостатинът все още осигурява инхибиторни импулси, а отрицателната обратна връзка на IGF-1 продължава да модулира изхода. Това е фундаменталната механистична разлика между тезаморелин и инжектирането на екзогенен GH.
Защо пулсативността има значение за загубата на мазнини
Екзогенният GH осигурява непрекъсната, супрафизиологична експозиция. Тезаморелин осигурява усилен, но все пак пулсативен изход на GH. Това разграничение има измерими последици надолу по веригата:
- Висцералните адипоцити експресират по-висока плътност на GH рецептори и β-адренергични рецептори в сравнение с депата на подкожна мастна тъкан
- Пулсативният GH преференциално активира хормон-чувствителната липаза (HSL) в тези висцерални депа
- GH антагонизира антилиполитичното действие на инсулина, като този ефект е по-силно изразен във висцералните мазнини
- Непрекъснатата експозиция на GH (екзогенен) води до по-силна инсулинова резистентност и по-равномерна мобилизация на мазнини във всички депа
Крайният резултат: тезаморелин мобилизира висцералните мазнини с относителна селективност, докато екзогенният GH засяга висцералните и подкожните мазнини по-равномерно — с цената на значително по-лоши странични ефекти върху глюкозния метаболизъм.
Оста на IGF-1
Пулсативното освобождаване на GH стимулира чернодробното производство на IGF-1, което медиира много от анаболните и насърчаващи растежа ефекти на GH. Всички големи изпитвания на тезаморелин документират постоянно повишаване на IGF-1. IGF-1 също така осигурява отрицателна обратна връзка както в хипофизата, така и в хипоталамуса, създавайки самоограничаваща се система — още едно предимство в безопасността спрямо екзогенния GH, който напълно потиска производството на ендогенен GH.
Клинични доказателства: Намаляване на висцералните мазнини
Основният набор от данни
Най-силните доказателства за тезаморелин идват от две знакови рандомизирани, плацебо-контролирани изпитвания при свързана с ХИВ липодистрофия:
- Falutz et al., 2007 (NEJM): Демонстрира значително намаляване на VAT, измерено чрез КТ скенер, в продължение на 26 седмици
- Falutz et al., 2010 (NEJM): Разширени данни, потвърждаващи 15–18% намаление на висцералната мастна тъкан спрямо плацебо за период от 6–12 месеца
Тези изпитвания са използвали златния стандарт за измерване на VAT чрез КТ като първична крайна точка — а не обиколка на талията или ИТМ, които са груби заместители. Ефектът е бил специфичен: висцералните мазнини са намалели значително, докато подкожната мастна тъкан е показала минимална промяна. Тази тъканна селективност е определящата клинична характеристика на съединението.
Ключови клинични резултати
Резултат | Мащаб | Ниво на доказателство |
|---|---|---|
Намаляване на VAT (измерено с КТ) | 15–18% спрямо плацебо | Фаза 3 RCT (висока увереност) |
Подобрение на триглицеридите | Значително намаление | Вторична крайна точка (средно-висока) |
CRP / възпалителни маркери | Подобрени | Вторична крайна точка (средно-висока) |
Каротидна IMT (дебелина интима-медия) | Благоприятна тенденция | Вторичен анализ (средна) |
Повишаване на IGF-1 | Постоянно увеличение | Всички изпитвания (висока увереност) |
Намаляване на подкожните мазнини | Минимално / незначително | Данни от Фаза 3 (висока увереност — това е функция, а не ограничение) |
Маркери за сърдечно-съдов риск
Вторичните анализи от изпитванията за ХИВ-липодистрофия показват подобрения в триглицеридите, С-реактивния протеин и дебелината на интима-медия на сънната артерия. Механизмът е двоен: директни ефекти на GH/IGF-1 върху липидния метаболизъм и ендотелната функция, плюс индиректна полза от намаляването на висцералната мазнина — метаболитно активен ендокринен орган, който секретира провъзпалителни адипокини (TNF-α, IL-6, резистин).
Проблемът с отмиването (Washout Problem)
Критично откритие от клиничните изпитвания: намаляването на VAT се обръща бързо след прекратяване на лечението. Периодите на отмиване са показали, че висцералните мазнини се връщат към изходните нива в рамките на месеци след спирането на тезаморелин. Това има големи практически последици — тезаморелин функционира като хронична терапия, а не като краен "цикъл" в традиционния смисъл на пептидната общност.
Намаляване на чернодробните мазнини
GH директно намалява чернодробната de novo липогенеза и насърчава β-окислението на мастни киселини. IGF-1 може допълнително да подобри чернодробната инсулинова чувствителност, намалявайки натрупването на липиди.
- Stanley et al., 2014 (J Clin Endocrinol Metab): Демонстрира намаляване на чернодробните мазнини при ХИВ пациенти със съпътстваща NAFLD
- Dichtel et al., 2022: Малко, едноцентрово пилотно проучване, показващо намаляване на чернодробните мазнини при пациенти с NAFLD без ХИВ — първите данни, предполагащи полза извън ХИВ популацията
Това е обещаваща, но ранна област. Фаза 2b/3 изпитвания за NAFLD/NASH без ХИВ се очакват в рамките на 2–5 години. Механистичната обосновка е силна, но настоящият набор от данни не е достатъчен, за да се препоръча тезаморелин като лечение за NAFLD извън клинични изпитвания.
Когнитивни ефекти: Проучванията на Vitiello
GHRH рецепторите се експресират в хипокампуса и други мозъчни региони, участващи в консолидацията на паметта. Това осигурява правдоподобен, директен невромеханистичен път — отделно от системните ефекти на IGF-1 върху телесния състав.
Vitiello et al., 2014 проведоха малки пилотни проучвания при по-възрастни възрастни и при пациенти с леко когнитивно увреждане. Резултатите показаха подобрена вербална памет при прилагане на GHRH аналог. Предполагаемият механизъм включва повишена синаптична пластичност, неврогенеза и церебрален глюкозен метаболизъм чрез директен агонизъм на GHRHR в мозъка.
Статус на доказателствата: Интригуващи, но предварителни. Това са били малки пилотни проучвания. Не са провеждани големи, потвърждаващи рандомизирани контролирани изпитвания. Изследванията в тази област изглежда са в застой — няма големи публикации, които да са развили хипотезата за когнитивната полза след първоначалните пилотни проекти. Интересът на биохакинг общността към тезаморелин като "ноотропик" в момента е спекулативна екстраполация от недостатъчно подкрепени данни.
Ключовият неотговорен въпрос: превръща ли се наблюдаваното когнитивно подобрение в клинично значима превенция или забавяне на деменцията? Отговорът на това би изисквал 1–2 годишно RCT при пациенти с MCI или ранен Алцхаймер, използвайки стандартизирани когнитивни батерии и невроизобразяващи биомаркери.
Дозиране, приложение и практически протоколи
Протокол, одобрен от FDA
- Доза: 2 mg/ден
- Път на въвеждане: Подкожна инжекция (корем, редуване на местата на инжектиране)
- Време: Веднъж дневно, обикновено сутрин на гладно (за да се избегне притъпяването на освобождаването на GH от постпрандиалния инсулин)
- Продължителност: Безсрочно за одобреното показание, като се има предвид обръщането на VAT при спиране
Техника на инжектиране
Реконституирайте лиофилизирания прах с предоставения разредител. Инжектирайте подкожно в корема, като избягвате зоната на пъпа. Редувайте местата на инжектиране, за да сведете до минимум липохипертрофията. Стандартните инсулинови спринцовки (29–31 gauge) са типични.
Извън предписанията (Off-Label) / Биохакинг протоколи
Общността е разработила циклиращи протоколи при липса на официални клинични насоки:
- 5 дни прием / 2 дни почивка — общ протокол за управление на разходите и теоретичната десенсибилизация на рецепторите
- 3-месечни цикли с 1-месечни почивки — друг широко обсъждан подход
- По-ниски дози (1–1,5 mg/ден) — някои потребители намаляват дозата, за да управляват страничните ефекти или разходите
Важно предупреждение: Нито един от тези протоколи няма подкрепа от клинични изпитвания. Данните за отмиване (washout) от контролирани изпитвания предполагат, че прекъсванията в терапията могат да компрометират ефикасността. Парадигмите за циклиране, заимствани от други пептидни контексти, може да не се прилагат за съединение, чиито ползи изискват продължително приложение.
Сравнение с други GH секретагози
Характеристика | Тезаморелин | Серморелин | CJC-1295 (с DAC) | Екзогенен GH |
|---|---|---|---|---|
Механизъм | GHRH аналог | Фрагмент от GHRH (1-29) | Модифициран GHRH + свързване с албумин | Директен агонист на GH рецептора |
Полуживот | ~30–50 мин | ~10 мин | Дни (свързан с албумин) | Часове |
Модел на секреция на GH | Пулсативен | Пулсативен | Продължителен (непулсативен) | Непулсативен |
Честота на инжектиране | Веднъж дневно | 1–3 пъти дневно | 1–2 пъти седмично | Дневно |
Одобрено от FDA | Да (ХИВ липодистрофия) | Не (прекратено) | Не | Да (многобройни показания) |
Клинични данни при хора | Стабилна Фаза 3 | Ограничени | Минимални | Обширни |
Селективност към VAT | Висока | Предполагаемо сходна | Неизвестна | По-ниска (засяга всички депа) |
Риск от инсулинова резистентност | По-нисък | По-нисък | Неизвестен | По-висок |
Цена | Висока ($$$) | Умерена ($$) | Ниска–Умерена ($–$$) | Променлива ($–$$$$) |
Статус в WADA | Забранен (S2) | Забранен (S2) | Забранен (S2) | Забранен (S2) |
Защо Тезаморелин пред екзогенен GH за висцерални мазнини
Обосновката е ясна: тезаморелин постига сравнимо или по-добро намаляване на висцералните мазнини със значително по-добър профил на метаболитни странични ефекти. Екзогенният GH потиска ендогенното производство, осигурява нефизиологична продължителна експозиция, води до по-силна инсулинова резистентност и липсва тъканна селективност. За специфичната цел за намаляване на висцералната мастна тъкан, като същевременно се запазва глюкозният толеранс, тезаморелин е механистично и клинично по-добрият инструмент.
Странични ефекти и профил на риска
Чести странични ефекти
- Реакции на мястото на инжектиране (еритема, сърбеж, болка) — най-често съобщаваните
- Артралгия / болка в ставите — свързана с повишаването на GH/IGF-1, обикновено лека
- Периферен оток — задържане на течности, зависимо от дозата
- Парестезия — изтръпване/мравучкане, обикновено преходно
Метаболитни опасения
- Повишаване на глюкозата — случва се, но обикновено е по-малко тежко, отколкото при екзогенния GH. Пациенти с предшестваща инсулинова резистентност или диабет се нуждаят от наблюдение
- Повишаване на IGF-1 — хроничният супрафизиологичен IGF-1 носи теоретичен риск от насърчаване на клетъчната пролиферация. В клиничните изпитвания не се е появил сигнал за рак, но продължителността на изпитванията (1–2 години) е недостатъчна за оценка на дългосрочния онкологичен риск
Неизвестното: Дългосрочна безопасност при здрави популации
Всички данни за безопасност произтичат от ХИВ-позитивни пациенти за продължителност на проучванията от 1–2 години. Няма никакви данни за дългосрочна безопасност при здрави, застаряващи възрастни, използващи тезаморелин извън предписанията (off-label) за телесен състав, когнитивни функции или дълголетие. Теоретичните рискове от продължителното повишаване на IGF-1 — ускорена клетъчна пролиферация, потенциален онкологичен риск — остават количествено неопределени в тази популация. Това е най-голямата празнина в доказателствата за употреба извън предписанията.
Регулаторен и антидопингов статус
- FDA: Одобрен само за свързана с ХИВ липодистрофия (Egrifta). Всички други употреби са извън предписанията
- DEA: Контролирано вещество от списък IV в САЩ
- WADA: Забранен по всяко време в категория S2 — Фактори, освобождаващи растежен хормон. Тестваните спортисти не могат да използват това съединение по време на състезание или извън него
- Застраховка: Като цяло се покрива само за одобреното показание; употребата извън предписанията обикновено изисква плащане в брой при значителни разходи
Резюме на риска и ползата по популация
Популация | Полза | Профил на риска | Нетна оценка |
|---|---|---|---|
ХИВ+ с липодистрофия (одобрено) | 15–18% намаление на VAT, подобрени CV маркери | Управляеми странични ефекти, установени данни за безопасност | Благоприятна |
NAFLD/NASH без ХИВ | Обещаващо намаляване на чернодробните мазнини | Ограничени данни, off-label, висока цена | Неутрална — обещаваща, но преждевременна |
Здрави биохакери / против стареене | Теоретично намаляване на VAT, спекулативни когнитивни ползи | Няма данни за дългосрочна безопасност, неизвестна ефикасност, висока цена, правна сложност | Недостатъчни данни |
Състезаващи се спортисти | Представяне и телесен състав | Забранено вещество, край на кариерата, ако бъде открито | Противопоказано (регулаторно) |
Ключови изводи
- Модификацията на транс-3-хексенова киселина на тезаморелин е структурната основа за неговата клинична полезност — без нея имате фармакокинетичните ограничения на серморелин
- Запазването на пулсативната секреция на GH не е маркетингова точка; това е механистичната причина за селективността към VAT и по-добрия метаболитен профил на страничните ефекти спрямо екзогенния GH
- Доказателствата от Фаза 3 за намаляване на висцералните мазнини при ХИВ-липодистрофия са солидни и възпроизводими — това е крепостта на доказателствата за съединението
- Всичко останало — когнитивни функции, NAFLD без ХИВ, общо действие против стареене — е екстраполация от пилотни данни, механистични разсъждения или анекдоти от общността
- Намаляването на VAT се обръща след спиране, което прави тезаморелин хронична терапия, а не пептид, който може да се циклира
- Никакви знакови клинични изпитвания между 2024–2026 г. не са променили съществено този пейзаж на доказателствата
- Ентусиазмът в общността значително изпреварва клиничните данни за приложения извън предписанията (off-label)
Бъдещи насоки
Най-вероятното клинично развитие в близко бъдеще е разширяване в посока NAFLD/NASH без ХИВ, където механистичната обосновка и пилотните данни съвпадат. Изследванията на когнитивните ползи може да видят подновен интерес с нарастването на областта на изследванията на метаболитно-мозъчната ос, но понастоящем им липсва финансиране и импулс за окончателни изпитвания. Формулация с дълго действие би трансформирала практическото изчисление за хронична употреба, но няма публично известна подобна програма. Генеричната конкуренция не е неизбежна поради патентната защита, което поддържа разходите високи в обозримо бъдеще.