Трипептид KPV: Противовъзпалително заздравяване на червата
Механизми, изследвания при IBD и протоколи
Въведение
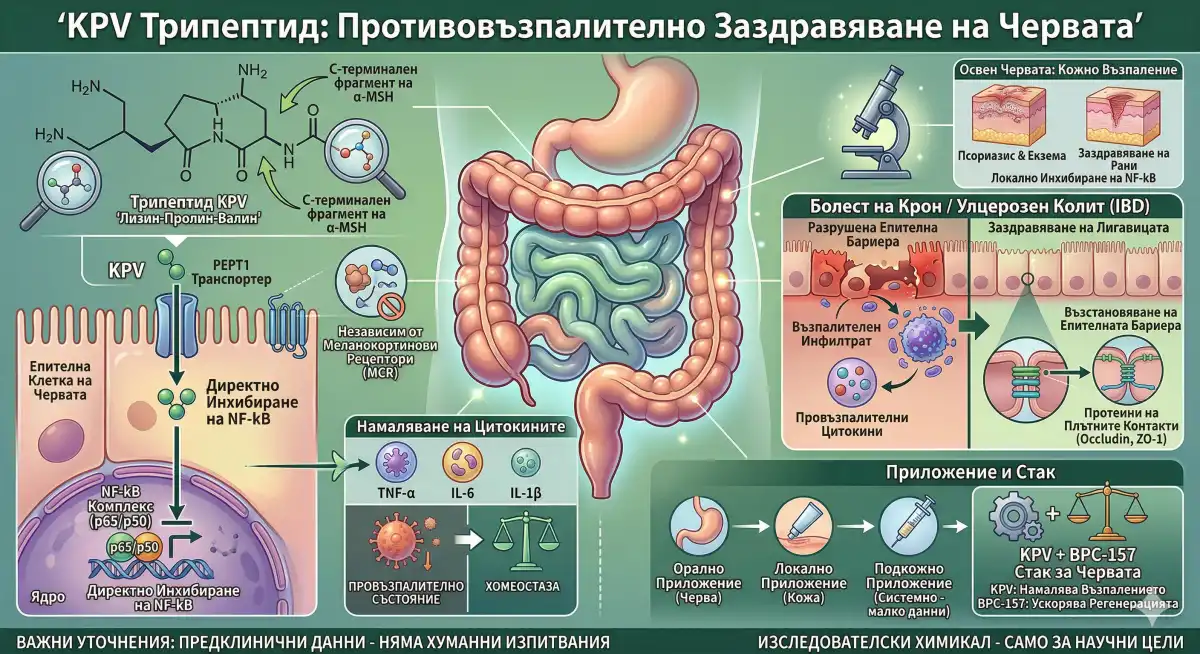
KPV е С-терминален трипептиден фрагмент на алфа-меланоцит стимулиращия хормон (α-MSH), състоящ се от три аминокиселини: лизин-пролин-валин. За разлика от пълната молекула на α-MSH или синтетичните меланокортинови агонисти като Melanotan II, KPV действа чрез фундаментално различен механизъм — такъв, който напълно заобикаля меланокортиновите рецептори и вместо това се насочва към възпалителната каскада в нейния транскрипционен корен. За биохакинг общността основната привлекателност на KPV е ясна: той преживява орално приложение, натрупва се в дебелото черво и директно инхибира един от главните възпалителни превключватели в тялото.
Тази статия разглежда молекулярния механизъм, предклиничните доказателства за заздравяване на червата и кожно възпаление, сравнява KPV със сродни съединения и предоставя практически протоколи — като същевременно ясно посочва къде доказателствата са силни и къде липсват.
Механизъм на действие: Директно инхибиране на NF-κB
Вътреклетъчно проникване и независимост от рецептори
Механизмът на KPV се отличава от почти всяко друго съединение, получено от α-MSH. Пълната дължина на α-MSH упражнява своите противовъзпалителни ефекти чрез свързване с меланокортинов рецептор 1 (MC1R) на клетъчната повърхност, предизвиквайки сигнализация надолу по веригата. KPV напълно пропуска тази стъпка.
Вместо това, KPV влиза в имунните и епителните клетки чрез пептидни транспортери — по-специално PEPT1, същият транспортер, участващ в абсорбцията на хранителни пептиди. Веднъж попаднал вътре в клетката, той взаимодейства директно със сигналния комплекс NF-κB. Това е демонстрирано in vitro от Brzoska et al. (2008), които показват, че KPV запазва своята противовъзпалителна активност в клетки без функционални меланокортинови рецептори — потвърждавайки, че механизмът му е независим от рецепторите.
Това не е маловажна разлика. То означава:
- Няма меланотропни ефекти — няма почерняване, няма промени в пигментацията.
- Няма модулация на апетита или либидото — странични ефекти, свързани с MCR агонисти като MT-II.
- По-предсказуемо действие на тъканно ниво — ефектът се определя от вътреклетъчната концентрация, а не от плътността на рецепторите или полиморфизма.
Блокиране на ядрената транслокация на NF-κB p65
Основната молекулярна мишена е р65 субединицата на NF-κB. При нормална възпалителна сигнализация, NF-κB комплексът (обикновено p65/p50) се задържа в цитоплазмата от инхибиторни IκB протеини. Когато клетката получи възпалителен стимул (LPS, TNF-α, IL-1β), IκB се фосфорилира и разгражда, освобождавайки p65 да се транслокира в ядрото и да активира транскрипцията на провъзпалителни гени.
KPV се намесва в тази стъпка на транслокация. Kang et al. (2006) демонстрират в проучвания на клетъчни линии, че KPV предотвратява навлизането на p65 в ядрото — или чрез стабилизиране на взаимодействието с IκB, или чрез намеса в сигналите за ядрен импорт на самия p65. Точното място на свързване все още се изследва, но функционалният резултат е ясен и възпроизводим в множество клетъчни типове.
Потискане на цитокините надолу по веригата
С блокирането на p65 извън ядрото, транскрипцията на неговите мишени надолу по веригата се потиска. Практическият резултат е намалено производство на:
- TNF-α — централен двигател на тъканно увреждане при IBD и системно възпаление.
- IL-6 — участва в отговора на острата фаза и хроничната възпалителна сигнализация.
- IL-1β — ключов медиатор на активирането на вродения имунитет и пироптозата.
Dalmasso et al. (2008) потвърждават това намаляване на цитокините в модел на колит, индуциран от декстран сулфат натрий (DSS), показвайки дозозависимо намаляване на трите маркера в тъканта на дебелото черво. Zheng et al. (2015) наблюдават сравнимо потискане на цитокините в модели на кожно възпаление.
Изследвания при IBD: Модели на колит и заздравяване на лигавицата
Данните за DSS колита
Най-силните предклинични доказателства за KPV идват от модели на колит при гризачи, по-специално модела DSS — добре установен заместител на улцерозен колит, който произвежда епително увреждане, възпалителна инфилтрация и дисфункция на бариерата.
Dalmasso et al. (2008) публикуват знаковото проучване: оралното приложение на KPV при мишки, третирани с DSS, води до:
- Значително намаляване на оценките за хистологично увреждане — по-малко разрушаване на криптите, по-малко възпалителен инфилтрат.
- Намалени нива на TNF-α, IL-6 и IL-1β в тъканта на дебелото черво.
- Възстановяване на целостта на епителната бариера — измерено чрез експресия на протеини на плътните контакти (occludin, ZO-1).
- Намалена загуба на тегло и индекс на активност на заболяването в сравнение с нетретираните контроли.
Ефектът е дозозависим и статистически значим по множество показатели.
Възстановяване на епителната бариера
Освен просто намаляване на възпалението, KPV изглежда активно насърчава възстановяването на лигавицата. Механизмът включва:
- Резистентност към апоптоза в епителните клетки на криптите — запазване на регенеративната клетъчна популация.
- Увеличаване на регулацията на протеините на плътните контакти — по-специално occludin и ZO-1, критични за парацелуларната бариерна функция.
- Повишена пролиферация на епителните клетки — ускоряване на обновяването, необходимо за затваряне на празнините в лигавицата.
Тази комбинация от противовъзпалителна и възстановителна активност прави KPV особено интересен за приложения в червата. Той не просто потиска имунния отговор — той създава условия за структурно възстановяване.
Орална бионаличност: Ключовото предимство
Трипептидната структура на KPV придава необичайна устойчивост на протеолитично храносмилане. Проучвания, използващи радиоактивно белязан KPV при гризачи (базирани на работата на Luger и колеги през 90-те и 2000-те години), демонстрират, че пептидът преживява стомашната киселина и панкреатичните ензими, преминава през тънките черва до голяма степен непокътнат и се натрупва в тъканта на дебелото черво.
Това е критично практическо предимство. Повечето биоактивни пептиди (включително BPC-157 до известна степен, и със сигурност по-големи пептиди като TB-500) се сблъскват със значително разграждане в горната част на стомашно-чревния тракт. Малкият размер на KPV и специфичната аминокиселинна последователност го правят един от малкото пептиди, при които оралното приложение е наистина жизнеспособен път за локални стомашно-чревни ефекти.
Важно уточнение: Тези данни за стабилност и натрупване са от животински модели. Фармакокинетични данни за хора — абсолютна орална бионаличност, тъканни концентрации, полуживот — не съществуват в публикуваната литература. Настоящите протоколи за орално дозиране са екстраполации.
Кожно възпаление и заздравяване на рани
Инхибирането на NF-κB от KPV не е ограничено само до червата. Локалното приложение е изследвано при животински модели на кожно възпаление с обещаващи резултати.
Zheng et al. (2015) изследват KPV в псориазиформени и екзематозни кожни модели, откривайки:
- Намален възпалителен инфилтрат в дермалната тъкан.
- Намалено локално производство на цитокини и хемокини в кератиноцитите.
- Ускорено затваряне на рани в сравнение с контролите, третирани само с носител.
Предложеният механизъм е прост: локалното потискане на NF-κB в кератиноцитите и дермалните имунни клетки модулира възпалителната микросреда и може косвено да подпомогне ангиогенезата и реепителизацията.
За практически цели, локалният KPV предлага потенциална нестероидна опция за локализирани възпалителни кожни състояния. Базата от доказателства е по-слаба отколкото за приложения в червата, но механизмът е последователен и рисковият профил за локална употреба е нисък.
KPV срещу сродни съединения
Характеристика | KPV | Пълна дължина α-MSH / MT-II | BPC-157 |
|---|---|---|---|
Произход | Естествен фрагмент на α-MSH | Ендогенен хормон / синтетичен аналог | Синтетичен пептид от стомашен сок |
Основен механизъм | Инхибиране на NF-κB p65 (вътреклетъчно) | Активиране на MCR-1 (рецепторно-медиирано) | Ангиогенеза, синтез на NO, сигнализация на растежни фактори |
Зависим от рецептор? | Не | Да (MCR-1) | Неясно / множество пътища |
Орална бионаличност | Висока (стабилност на трипептида) | Лоша (разгражда се) | Умерена (дискутирана) |
Меланотропни ефекти | Няма | Да (почерняване, апетит, либидо) | Няма |
Най-добър случай на употреба | Локално стомашно-чревно възпаление, локално за кожа | Системно противовъзпалително, почерняване | Широко заздравяване на тъкани (черва, сухожилия, връзки) |
Клинични данни при хора | Няма | Ограничени (MT-II за сексуална дисфункция) | Няма (специфично за BPC-157) |
KPV + BPC-157: Стак за червата
Комбинацията от KPV и BPC-157 за възстановяване на червата е механистично рационална и широко обсъждана в биохакинг общностите. Логиката:
- KPV се справя с възпалителния компонент — потиска имуно-медиираното увреждане.
- BPC-157 се справя с възстановителния компонент — насърчава ангиогенезата, сигнализацията на растежните фактори и медиираното от азотен оксид възстановяване на тъканите.
Това са допълващи се, а не припокриващи се механизми. На теория KPV намалява текущото увреждане, докато BPC-157 ускорява структурното възстановяване.
Реалността на доказателствата: Нито едно контролирано проучване — върху животни или хора — не е тествало тази комбинация. Обосновката е изцяло механистична екстраполация плюс анекдоти от общността. Анекдотичните съобщения от пептидни форуми са като цяло положителни, но неконтролирани и подлежащи на плацебо ефекти и объркващи фактори. Това е протокол с висок потенциал, но с висока степен на несигурност.
Практически протоколи
Критичен отказ от отговорност: Всички дозировки по-долу са екстраполирани от проучвания върху животни и практики на общността. Не съществуват фармакокинетични или клинични данни за хора за KPV. Това не са медицински препоръки.
Орално приложение (Заздравяване на червата)
Това е най-силният случай на употреба на KPV, с най-добра механистична и предклинична подкрепа.
- Диапазон на дозата: 200–500 mcg, 1–2 пъти дневно
- Време: На гладно (намалява конкуренцията за пептиден транспорт)
- Продължителност: 4–8 седмични цикли
- Цикличност: 4 седмици прием / 2 седмици почивка, или 8 седмици прием / 4 седмици почивка
- Забележки: Някои потребители съобщават за полза в долната граница; по-високи дози (до 1000 mcg) се появяват в протоколите на общността, но липсва допълнителна предклинична подкрепа за пропорционално по-голям ефект.
Локално приложение (Кожа)
- Формулировка: KPV, разтворен в подходящ носител (обикновено бактериостатична вода, прилагана директно, или смесен в проста кремообразна основа)
- Доза: 100–300 mcg на приложение върху засегнатата област
- Честота: 1–2 пъти дневно
- Продължителност: До отзвучаване или за определени 4-седмични цикли
- Забележки: Очаква се минимална системна абсорбция; метод с най-нисък риск.
Подкожна инжекция (Системно)
- Диапазон на дозата: 200–500 mcg, 1 път дневно
- Продължителност: Само кратки цикли (2–4 седмици)
- Забележки: Това е методът с най-малко доказателства. Системните противовъзпалителни ефекти чрез SubQ KPV разчитат на теоретичен механизъм и минимални данни от животни. Профилът риск-полза е по-малко благоприятен от оралните или локалните пътища. Съществуват по-добре проучени алтернативи за управление на системно възпаление.
Комбиниран протокол: KPV + BPC-157 за възстановяване на червата
- KPV: 250–500 mcg орално, 2 пъти дневно на гладно
- BPC-157: 250–500 mcg орално, 2 пъти дневно (могат да се приемат заедно)
- Продължителност: 4–8 седмици
- Обосновка: Противовъзпалително (KPV) + про-заздравяващо (BPC-157) за цялостно възстановяване на чревната бариера.
- Ниво на доказателства: Само механистична обосновка + анекдоти от общността. Няма контролирани данни.
Общи насоки за цикличност
Цикличността се препоръчва по две причини:
- Неизвестни дългосрочни ефекти от хроничното потискане на NF-κB — NF-κB е фундаментален имунен път. Продължителното инхибиране теоретично би могло да наруши защитата на гостоприемника срещу инфекции.
- Липса на данни за безопасност при хора извън самоекспериментирането в общността — консервативното, циклично дозиране ограничава кумулативната експозиция, като същевременно позволява терапевтичен ефект.
Ограничения на доказателствата
Този раздел е важен. Биохакинг общността има склонност да компресира разстоянието между "работи в модел на колит при гризачи" и "лекува пропускливите ви черва". Ето къде всъщност стоят доказателствата:
Ниво на доказателства | Какво съществува | Увереност |
|---|---|---|
In vitro механизъм | Инхибиране на NF-κB p65, MCR независимост, потискане на цитокини | Висока — добре репликирано |
Животински модели на колит | Заздравяване на лигавицата, възстановяване на бариерата, намаляване на цитокини (DSS модел) | Средно-висока — последователно, зависимо от дозата |
Животински модели на кожа | Намалено възпаление, ускоряване на заздравяването на рани | Средна |
Орална бионаличност | Стабилност при храносмилане, натрупване в дебелото черво (проучвания с трасери при гризачи) | Средно-висока — но няма PK при хора |
Клинични изпитвания при хора | Няма публикувани | Неприложимо |
Системни подкожни ефекти | Теоретични + минимални данни от животни | Ниска |
Дългосрочна безопасност | Няма данни за нито един вид извън краткосрочните проучвания | Неизвестна |
Предклиничният пакет е наистина силен — KPV не е пожелателно мислене, изградено върху едно проучване. Но пропастта между колита при гризачи и човешкия IBD е съществена, а разликата между дозирането на "изследователски химикал" и оптимизираните човешки протоколи е напълно непокрита от официални данни.
Регулаторен статус и WADA
- Регулаторен: KPV е неодобрена лекарствена субстанция в САЩ, ЕС, Обединеното кралство и повечето юрисдикции. Продава се като "изследователски химикал" за употреба in vitro. Продажбата за човешка консумация не е законна на повечето пазари.
- WADA: KPV не е изрично посочен в Списъка на забранените вещества на WADA. Въпреки това, неговият противовъзпалителен механизъм теоретично би могъл да попадне в духа на антидопинговите правила, ако се използва в контекста на състезания. Спортистите, подлежащи на тестване, трябва да третират това като сива зона и да проявяват повишено внимание.
Изследователски перспективи
Малко вероятно е KPV да види официално фармацевтично разработване или мащабни клинични изпитвания в близко бъдеще. Като естествен трипептид, той не може да бъде патентован, което премахва търговския стимул за скъпи изпитвания върху хора. Напредъкът вероятно ще дойде от:
- Академични проучвания за оптимизирани системи за доставка (капсулиране с наночастици, ентерични покрития).
- Изследвания на комбинации с пробиотици или допълващи пептиди.
- Ex vivo изследвания на човешки тъкани, които преодоляват празнината от животни към хора, без да изискват пълни клинични изпитвания.
- Продължаващо натрупване от общността на анекдотични данни.
Най-въздействащото развитие би било малко пилотно проучване при лек улцерозен колит или пациенти с локален псориазис — нещо, което би могло да се осъществи със скромно финансиране и би променило драматично пейзажа на доказателствата.
Ключови изводи
- Основният механизъм на KPV — независимо от рецептора, вътреклетъчно инхибиране на NF-κB p65 — е добре установен in vitro и осигурява чист противовъзпалителен ефект без меланокортинови странични ефекти.
- Оралната бионаличност и натрупването в дебелото черво го правят уникално практичен за стомашно-чревни приложения сред пептидите.
- Данните за колит при животни са последователни и убедителни: заздравяване на лигавицата, намаляване на цитокините, възстановяване на бариерата.
- Не съществуват никакви клинични изпитвания върху хора — всички протоколи са екстраполации.
- Оралното дозиране за заздравяване на червата е най-добре подкрепеният случай на употреба; локалното за кожата е разумно; SubQ за системни ефекти е слабо подкрепено.
- Стакът KPV + BPC-157 е механистично рационален, но напълно нетестван в контролирани условия.
- Цикличността е благоразумна предвид неизвестните дългосрочни ефекти от хроничната модулация на пътя на NF-κB.
- Качеството на източника има значение — като нерегулиран изследователски химикал, проверката на чистотата е от съществено значение.