Тимозин Алфа-1
Механизми на имунна модулация, клинични доказателства и терапевтични протоколи
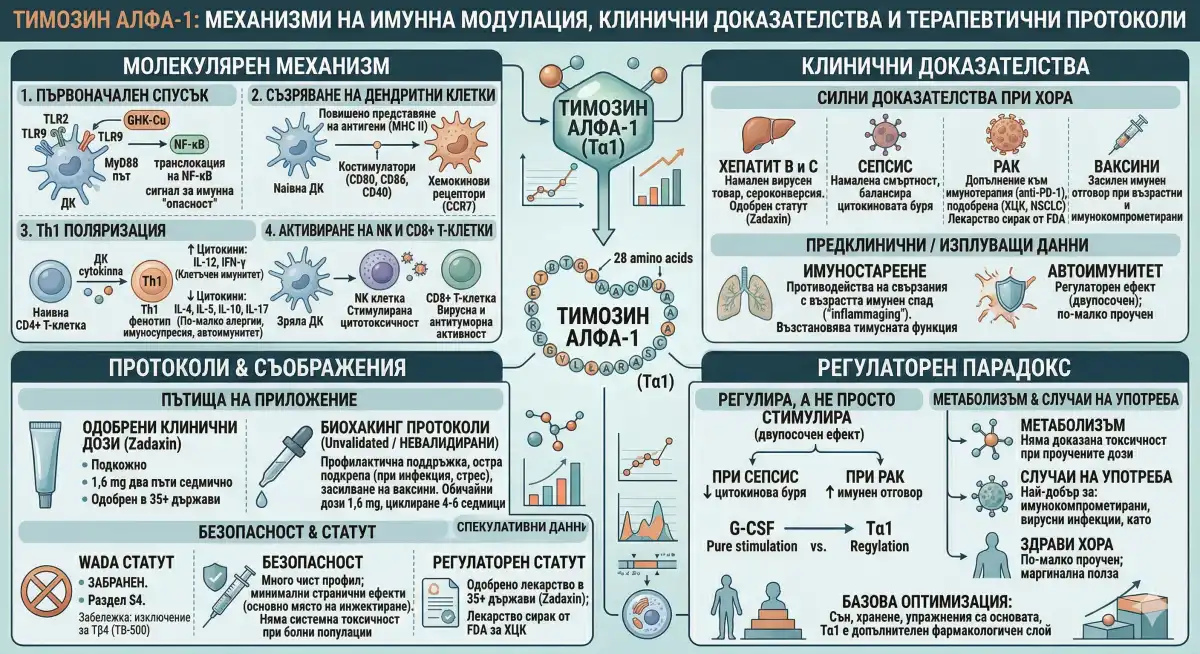
Въведение
Тимозин Алфа-1 (Tα1) заема рядка позиция в пейзажа на пептидите: това е едно от малкото съединения, обсъждани в биохакинг средите, което всъщност има официални одобрения като лекарство, статут на лекарство сирак и значителен обем от данни от клинични изпитвания при хора зад гърба си. Предлаган на пазара като Zadaxin, Tα1 е одобрен за лечение на хепатит B и C в над 35 държави и има статут на лекарство сирак от FDA за хепатоцелуларен карцином (ХЦК) в Съединените щати.
За разлика от BPC-157 или Ipamorelin, където базата от доказателства е доминирана от животински модели и анекдоти, Tα1 осигурява истинска основа от данни за безопасност и ефикасност при хора — макар и при болни популации. Основният въпрос за потребителя, ориентиран към оптимизация, е дали драматичното възстановяване на имунитета, наблюдавано при имунокомпрометирани пациенти, се превръща в значими ползи за някой, чиято имунна система вече функционира добре.
Тази статия разглежда молекулярния механизъм, прави преглед на клиничните доказателства по показания, обхваща практическите протоколи за дозиране и идентифицира къде данните реално подкрепят употребата спрямо това къде се правят екстраполации.
Биохимичен механизъм на действие
Tα1 е пептид от 28 аминокиселини, произвеждан ендогенно от тимусната жлеза. Неговият механизъм не е "чук" с един-единствен път на действие — той представлява мултирецепторна оркестрация както на вродения, така и на придобития имунитет. Разбирането на тази каскада е от съществено значение за вземането на информирани решения за това кога и защо да се използва.
Активиране на TLR2/TLR9: Първоначалният спусък
Основното събитие нагоре по веригата след подкожно приложение на Tα1 е активирането на Toll-подобен рецептор 2 (TLR2) и Toll-подобен рецептор 9 (TLR9) върху дендритните клетки (DC) и други антиген-представящи клетки. Активирането на TLR2 сигнализира чрез пътя MyD88, което води до транслокация на NF-κB — главен транскрипционен фактор за възпалителна и имунна генна експресия. TLR9, който класически разпознава CpG ДНК мотиви, също се ангажира, въпреки че точното взаимодействие на свързване с Tα1 може да е непряко или да се случва на отделно място, вместо да имитира CpG олигонуклеотид (Romani et al., 2006; Serafino et al., 2012).
Това двойно ангажиране на TLR ефективно действа като сигнал за опасност, подготвяйки вродената имунна система така, сякаш е открита патогенна заплаха.
Ниво на доказателства: Силни in-vitro данни. Висока увереност в TLR2/9 като функционални цели.
Съзряване на дендритните клетки и представяне на антигени
Надолу по веригата след активирането на TLR, дендритните клетки претърпяват съзряване:
- Регулация нагоре на MHC клас II и костимулаторни молекули (CD80, CD86, CD40) на повърхността на DC
- Повишена експресия на хемокинови рецептори (най-вече CCR7), улесняваща миграцията на DC до лимфните възли
- Трансформация от състояние на покой към активно състояние, което позволява ефективно представяне на антигена на наивни Т-клетки
Тази стъпка е критична: дендритните клетки са мостът между вроденото откриване и придобития имунен отговор. Без зрели, активирани DC, отговорите на Т-клетките остават притъпени.
Ниво на доказателства: In-vitro проучвания и проучвания при животни. Средна увереност.
Th1 поляризация: Основното имунно изместване
Дендритните клетки, обусловени от Tα1, произвеждат различен цитокинов профил, който насочва наивните CD4+ T-клетки към Th1 фенотип:
Цитокин | Посока | Ефект |
|---|---|---|
IL-12 | ↑ Повишен | Стимулира Th1 диференциацията |
IFN-γ | ↑ Повишен | Засилва клетъчно-медиирания имунитет |
IL-4 | ↓ Намален | Намалява Th2 (алергия/атопия) сигнализирането |
IL-5 | ↓ Намален | Намалява активирането на еозинофилите |
IL-10 | ↓ Намален | Намалява имуносупресивното сигнализиране |
IL-17 | ↓ Намален | Намалява Th17 (свързана с автоимунитет) активността |
Тази Th1 поляризация е фармакологичният център. Доминиращият Th1 имунитет стимулира клетъчно-медиираните отговори срещу вируси и вътреклетъчни патогени — точно това, което искате за борба с инфекции, изчистване на вирусни резервоари и подпомагане на антитуморното наблюдение (Billich, 2002).
Ниво на доказателства: In-vitro данни и данни от животни. Средна увереност за мащаба на ефекта при хора.
Активиране на NK клетки и CD8+ T-клетки
Богатата на IL-12/IFN-γ среда, генерирана от Tα1, мощно активира клетките Естествени убийци (NK), засилвайки освобождаването на цитотоксични гранули и убиването на целеви клетки. Пролиферацията и ефекторната функция на CD8+ цитотоксичните Т-лимфоцити също се стимулират, подобрявайки както вирусния клирънс, така и антитуморната активност.
Проучванията при хора при пациенти с хепатит В/С показват, че подобреният вирусен клирънс корелира с повишена активност на NK и CD8+ Т-клетките, осигурявайки непряко, но значимо клинично валидиране на този път.
Ниво на доказателства: Проучвания при животни плюс подкрепящи корелативни данни при хора. Средна увереност.
Регулаторният парадокс: Имунна настройка, не просто стимулация
Може би най-важното механистично прозрение: Tα1 е фундаментално регулаторен, а не просто стимулиращ. При сепсис — състояние на хипервъзпалителна цитокинова буря — Tα1 намалява прекомерното производство на TNF-α и IL-6, потенциално чрез инхибиране на излезли извън контрол вериги за обратна връзка на TLR сигнализирането и насърчаване на функцията на регулаторните Т-клетки (Treg). При рак — често характеризиращ се с локална имуносупресия — той засилва имунното активиране.
Тази двупосочна активност предполага, че Tα1 действа като "тунер" на имунната система, тласкайки функцията към хомеостаза, вместо сляпо да я усилва. Това прави неговите ефекти силно зависими от контекста и го отличава от грубите стимулиращи агенти като G-CSF.
Клинични доказателства по показания
Хепатит В и С
Най-силният набор от данни при хора съществува тук. Tα1 като Zadaxin е демонстрирал:
- Намален вирусен товар при пациенти с хроничен HBV и HCV
- Подобрени нива на HBeAg сероконверсия, когато се комбинира с интерферон-алфа
- Благоприятен профил на безопасност в множество мащабни клинични изпитвания
Тези резултати формираха основата за регулаторно одобрение в над 35 държави. Механизмът съответства директно на Th1 изместването и засилената активност на цитотоксичните лимфоцити, описани по-горе.
Ниво на доказателства: Солидни данни от клинични изпитвания при хора. Висока увереност за ефикасност в тази популация.
Допълнение към имунотерапия при рак
Tα1 е изследван като допълнителна терапия при няколко вида тумори:
- Хепатоцелуларен карцином (ХЦК): Статут на лекарство сирак от FDA. Подобрена преживяемост при комбиниране с химиотерапия/TACE в множество изпитвания.
- Недребноклетъчен рак на белия дроб (NSCLC): Допълнителната употреба с химиотерапия показва полза за преживяемостта в няколко проучвания.
- Меланом: По-ранни проучвания изследваха неговия имуностимулиращ потенциал, въпреки че данните тук са по-малко солидни.
Логиката е ясна: Tα1 засилва антитуморния имунен отговор, който химиотерапията и лъчетерапията често потискат. Текущи изпитвания във Фаза II/III изследват комбинацията с инхибитори на контролните точки (anti-PD-1/PD-L1), особено за имунологично "студени" тумори — резултати се очакват през 2025-2026 г.
Ниво на доказателства: Множество изпитвания при хора при специфични видове рак. Средна до висока увереност като допълнение.
Сепсис
Множество мета-анализи (включително скорошни публикации от 2023-2024 г.) подкрепят ролята на Tα1 за намаляване на смъртността при пациенти със сепсис. Неговият регулаторен механизъм — потискане на цитокиновата буря, като същевременно запазва насочения срещу патогена имунитет — се справя с фундаментално предизвикателство в интензивните грижи, където чистата имуносупресия (напр. кортикостероиди) носи компромиси.
Ниво на доказателства: Силни данни при хора от множество мета-анализи. Средна до висока увереност.
Потенциране на ваксини
Tα1 е демонстрирал засилени отговори на антитела, когато се прилага едновременно с ваксини срещу грип и хепатит В, предимно при възрастни и имунокомпрометирани популации. Понастоящем липсват данни за модерни иРНК ваксини (COVID-19, актуализирани грипни платформи) при здрави възрастни. Анекдотичните доклади от биохакери за подобрени отговори към ваксините са чести, но неконтролирани.
Ниво на доказателства: Съществуват данни при хора, но са ограничени до по-стари платформи за ваксини и популации в напреднала възраст. Ниска до средна увереност за екстраполация към здрави възрастни с модерни ваксини.
Имуностареене и възраст
Нарастващият изследователски интерес е насочен към потенциала на Tα1 да противодейства на свързания с възрастта имунен спад ("inflammaging"). Тимусът инволюира с възрастта, намалявайки ендогенното производство на Tα1. Екзогенното добавяне би могло теоретично да възстанови някои аспекти на младежката имунна функция. Очакват се официални клинични изпитвания в тази област през следващите 2-4 години.
Ниво на доказателства: Механистично правдоподобно. До голяма степен предклинични. Ниска увереност за специфични резултати при здрави възрастни хора.
Протоколи за дозиране и приложение
Одобрени клинични дози
Протокол | Доза | Честота | Продължителност | Контекст |
|---|---|---|---|---|
Хепатит В/С (Zadaxin) | 1,6 mg | Два пъти седмично | 6-12 месеца | Подкожна инжекция |
Допълнение при рак | 1,6 mg | Два пъти седмично | Продължителност на химио-цикъла | Подкожна инжекция |
Сепсис (остър) | 1,6 mg | Ежедневно | 5-7 дни (остра фаза) | Подкожна инжекция |
Биохакерски протоколи (Извлечени от общността)
Следните протоколи циркулират в общностите за оптимизация на пептиди. Никой от тях не е валидиран в контролирани изпитвания върху здрави индивиди:
- Профилактична поддръжка: 1,6 mg подкожно, два пъти седмично, циклиране 4-6 седмици прием / 2-4 седмици почивка
- Остра имунна подкрепа: 1,6 mg подкожно ежедневно в продължение на 5-7 дни при начало на заболяване или периоди на висока експозиция (пътуване, тежки тренировъчни блокове)
- Потенциране на ваксини: 1,6 mg подкожно в продължение на 3-5 дни преди и след ваксинация
Подкожната инжекция е стандартният път. Типични са местата за инжектиране в корема или делтоидния мускул. Препоръчва се ротация, за да се сведе до минимум дразненето на мястото.
Съображения за циклиране
Циклирането е теоретично важно, но емпирично неподкрепено при здрави потребители. Логиката:
- Непрекъснатата имунна стимулация крие риск от толерантност или изтощение — продължителното активиране на TLR може да регулира нагоре маркерите за изтощение (PD-1, TIM-3, LAG-3) върху лимфоцитите
- Клиничните данни използват дефинирани курсове на лечение, а не безкрайно приложение
- Не съществуват лонгитюдни данни за имунно профилиране за здрави индивиди, използващи Tα1 хронично
Разумен предпазен подход въз основа на наличните доказателства: използвайте дефинирани курсове вместо отворени протоколи и обмислете периодично тестване на имунни биомаркери (лимфоцитни субпопулации, функция на NK клетките), ако продължавате употребата.
Безопасност и странични ефекти
Tα1 има един от най-чистите профили на безопасност в клиничното пространство на пептидите:
- Реакции на мястото на инжектиране (зачервяване, лека болка): Най-често срещаното нежелано събитие, обикновено леко и преходно
- Няма съобщени значими системни странични ефекти в обширните бази данни от клинични изпитвания при популации с хепатит, рак и сепсис
- Няма съобщена имуносупресия, органна токсичност или хормонален дисбаланс в публикуваните изпитвания
Теоретични рискове за здрави потребители (невалидирани):
- Дългосрочна имунна толерантност или изтощение при хронична употреба без циклиране
- Непредсказуема модулация на съществуващи автоимунни заболявания поради изместване на Th1 профила
- Потенциално обостряне на недиагностициран автоимунитет
Общият сигнал за безопасност от клиничната употреба е успокояващ, но остава предупреждението: популациите в клиничните изпитвания са били болни. Изчислението на риска и ползата се променя, когато вече сте здрави и очакваната полза е маргинална.
Регулаторен статут и статус на WADA
- FDA: Статут на лекарство сирак за хепатоцелуларен карцином. Не е одобрен като общо терапевтично средство или добавка.
- Международен: Одобрен като лекарство с рецепта (Zadaxin) за хепатит B/C и имунна модулация в 35+ държави.
- WADA: Забранен. Включен в Раздел S4 (Хормонални и метаболитни модулатори) като тимозин. Забележка: Тимозин Бета-4 (TB-500) е изключението, посочено в списъка, а не Tα1. Спортистите в спортове, съобразени с WADA, не могат да използват това съединение.
- Снабдяване: На неодобрени пазари се предлага чрез специализирани аптеки (с рецепта) и доставчици на изследователски химикали. Проверката на чистотата (COA от трета страна) е от съществено значение предвид сивия пазар на повечето вериги за доставки.
Сравнение със свързани съединения
Характеристика | Тимозин Алфа-1 | Тимозин Бета-4 (TB-500) | G-CSF (Филграстим) |
|---|---|---|---|
Основно действие | Имуномодулация | Възстановяване на тъкани, ангиогенеза | Стимулиране на неутрофили |
Механизъм | TLR2/9 → DC → Th1 изместване | LRP1, свързване с актин | G-CSF рецептор → миелоидна пролиферация |
Регулаторен статут | Лекарство сирак от FDA, одобрено в 35+ държави | Няма одобрение за лекарство | Одобрено от FDA за неутропения |
Най-добър случай на употреба | Имунна дисфункция, вирусни заболявания, подкрепа при ваксини | Възстановяване на сухожилия/връзки, заздравяване на рани | Тежка неутропения, възстановяване след химиотерапия |
Профил на странични ефекти | Минимални (място на инжектиране) | Минимални (място на инжектиране) | Болки в костите, риск от възпаление |
Статус на WADA | Забранен | Посочено изключение | Забранен |
Tα1 и TB-500 често се бъркат или смесват в дискусиите за биохакинг. Това са механистично различни пептиди с неприпокриващи се основни приложения.
Практически изводи
- Tα1 е легитимно фармацевтично средство с реални клинични данни — не е изследователски химикал, маскиран като лекарство. Отнасяйте се към него съответно.
- Най-силният случай на употреба за биохакери вероятно е прилагането в острата фаза — по време на висок имунен стрес, пътуване, интензивни тренировъчни блокове или при начало на инфекция — вместо безкрайно профилактично дозиране. Това отразява клиничните протоколи, където по-високото ежедневно дозиране се справя с остри обостряния.
- Ефектът на имунна настройка зависи от контекста. Ако имунната ви система вече функционира добре, маргиналната полза може да е малка. Ако сте имуносупресирани, възстановявате се от заболяване или стареете с намаляваща тимусна функция, ефектът може да бъде значителен.
- Нито едно рандомизирано контролирано изпитване (RCT) не е тествало Tα1 за профилактична имунна подкрепа при здрави възрастни. Всеки профилактичен протокол, с който се сблъсквате, е екстраполация.
- Основополагащата имунна оптимизация — сън, хранене, управление на стреса, упражнения — остава интервенцията с най-високи доказателства за здрави индивиди. Tα1 е фармакологичен слой върху тази основа, а не неин заместител.
- Ако използвате, циклирайте отговорно: дефинирани курсове (4-6 седмици), наблюдавайте с кръвни изследвания, ако е възможно, и избягвайте безкрайна непрекъсната употреба, докато не се появят лонгитюдни данни за безопасност при здрави популации.
Заключение
Tα1 е сред пептидите с най-много доказателства, налични за имунна модулация, с механизъм, който е добре характеризиран на молекулярно ниво и валидиран в множество болестни състояния при хора. Неговата регулаторна природа — настройване, а не просто засилване на имунитета — го прави механистично привлекателен, но и по-труден за прогнозиране в отделни случаи. Пропастта между доказаната му ефикасност при имунокомпрометирани пациенти и предполагаемата му полезност при здрави оптимизатори остава критичният нерешен въпрос. Използвайте го с информирана прецизност, а не като имунен мултивитамин.